- TOP
- >
- 膵芽細胞への分化制御メカニズムの一端を解明、iPS細胞での糖尿病治療に期待
新着ニュース30件
2017年8月12日 14:30
京都大学のiPS細胞研究所「CiRA」は9日、豊田太郎講師、長船健二教授らの研究グループが、ES細胞やiPS細胞といったヒト多能性幹細胞から膵臓細胞への分化過程を解析し、膵臓のもととなる膵芽細胞への分化を制御するメカニズムの一端を解明することに成功したと発表しました。糖尿病などの膵臓関連疾患における再生医療の開発研究基盤として寄与する知見になるとみられます。
膵臓は、胎生期の後方前腸にある膵前駆細胞と呼ばれる1層のシートから膵芽と呼ばれる細胞の塊を作ることで、はじめてかたちとして認識できるものになるため、膵芽は膵臓の最初の組織と考えられます。よって膵芽細胞が、膵臓再生医療の基盤となる細胞源として期待されているのです。しかし、メカニズムが不明なままでは、安定性や効率など、改良の余地がある問題を乗り越えることができません。
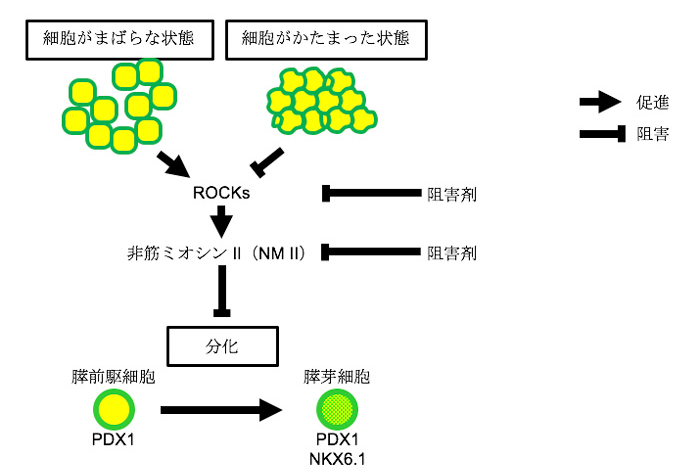
そこで研究グループは、この膵芽細胞への分化メカニズムを明らかにするため、細胞構造の変化に着目、細胞骨格の維持に関わるタンパク質の働きを阻害する低分子化合物を複数種類ヒトiPS細胞由来の膵前駆細胞に作用させたところ、ミオシン阻害剤の一種であるBlebbistatin(非筋ミオシンIIの阻害剤)や、ROCKに対するすべての阻害剤(Y-27632、Fasudil、GSK269962、H-1152)で処理した場合に、膵芽細胞への分化を観察できることを見出しました。
また、こうしたROCK阻害剤や非筋ミオシンII阻害剤(ROCK-NM II阻害剤)の膵芽細胞分化促進効果は、他のiPS細胞株やヒトES細胞でも確認できたそうです。
さらに、細胞密度が高い状態や細胞の塊のある状態など、分化に有利な培養条件で、ROCK活性やその下流にある非筋ミオシンIIの量がどうなっているか調べると、いずれも低下していることがわかり、ROCK-NM II阻害剤がこうした膵芽細胞の分化に有利な条件の細胞内状態を作り出したことから、分化の促進がみられたと考えられました。
研究グループでは、今回ヒトES細胞やiPS細胞から膵臓のもととなる膵芽への分化を促進する低分子化合物の同定に成功、同定した化合物が阻害するROCKや非筋ミオシン(NM II)の活性低下状態を作り出せば、膵前駆細胞から膵芽細胞への分化が活発に進むという制御のメカニズムを明らかにすることができたとまとめ、今後の糖尿病などに対する再生医療に寄与する、新たな知見が得られたとしています。
(画像はプレスリリースより)

京都大学 iPS細胞研究所 CiRA プレスリリース
http://www.cira.kyoto-u.ac.jp/
Stem Cell Reports : Rho-Associated Kinases and Non-muscle Myosin IIs Inhibit the Differentiation of Human iPSCs to Pancreatic Endoderm
http://www.cell.com/
【承認不要】志木市のむかしから今にいたるまでのことを知るなら郷土資料館(8月31日) 細胞の抗ストレス機能を利用した2型糖尿病治療薬の可能性を示唆(12月25日) 甘いのに低GI しかも完全オーガニックな食品が発売(12月24日) 患者自身の脂肪細胞を使う遺伝子治療 糖尿病への応用に期待(12月23日) 抗ストレス化合物に肥満や糖尿病軽減効果を確認 ドイツ(12月18日)

細胞骨格関連分子が関与
培養皿上でヒトiPS細胞から膵芽細胞への分化には、細胞密度が高い状態での培養や、細胞の塊を作ることが有効であることは、これまでの実験から明らかとなっていましたが、そのメカニズムについては依然不明でした。その一部を明らかにした、今回の研究グループによる成果をまとめた論文は、「Stem Cell Reports」オンライン版に8月8日付で掲載されています。膵臓は、胎生期の後方前腸にある膵前駆細胞と呼ばれる1層のシートから膵芽と呼ばれる細胞の塊を作ることで、はじめてかたちとして認識できるものになるため、膵芽は膵臓の最初の組織と考えられます。よって膵芽細胞が、膵臓再生医療の基盤となる細胞源として期待されているのです。しかし、メカニズムが不明なままでは、安定性や効率など、改良の余地がある問題を乗り越えることができません。
そこで研究グループは、この膵芽細胞への分化メカニズムを明らかにするため、細胞構造の変化に着目、細胞骨格の維持に関わるタンパク質の働きを阻害する低分子化合物を複数種類ヒトiPS細胞由来の膵前駆細胞に作用させたところ、ミオシン阻害剤の一種であるBlebbistatin(非筋ミオシンIIの阻害剤)や、ROCKに対するすべての阻害剤(Y-27632、Fasudil、GSK269962、H-1152)で処理した場合に、膵芽細胞への分化を観察できることを見出しました。
また、こうしたROCK阻害剤や非筋ミオシンII阻害剤(ROCK-NM II阻害剤)の膵芽細胞分化促進効果は、他のiPS細胞株やヒトES細胞でも確認できたそうです。
インスリンを分泌する成熟膵β細胞へ分化
ROCK-NM II阻害剤などで分化を促進して作った膵芽細胞は、マウスの生体内へ移植すると、胎生期の膵臓に似た組織構造が形成されるようになり、最終的には血糖値に応じてインスリンを分泌する、正常な成熟した膵β細胞へと分化しました。さらに、細胞密度が高い状態や細胞の塊のある状態など、分化に有利な培養条件で、ROCK活性やその下流にある非筋ミオシンIIの量がどうなっているか調べると、いずれも低下していることがわかり、ROCK-NM II阻害剤がこうした膵芽細胞の分化に有利な条件の細胞内状態を作り出したことから、分化の促進がみられたと考えられました。
研究グループでは、今回ヒトES細胞やiPS細胞から膵臓のもととなる膵芽への分化を促進する低分子化合物の同定に成功、同定した化合物が阻害するROCKや非筋ミオシン(NM II)の活性低下状態を作り出せば、膵前駆細胞から膵芽細胞への分化が活発に進むという制御のメカニズムを明らかにすることができたとまとめ、今後の糖尿病などに対する再生医療に寄与する、新たな知見が得られたとしています。
(画像はプレスリリースより)
京都大学 iPS細胞研究所 CiRA プレスリリース
http://www.cira.kyoto-u.ac.jp/
Stem Cell Reports : Rho-Associated Kinases and Non-muscle Myosin IIs Inhibit the Differentiation of Human iPSCs to Pancreatic Endoderm
http://www.cell.com/
-->
記事検索
アクセスランキング トップ10
特集
お問い合わせ